허가-신고증, 등록증, 승인서, 지정서, 판정서 등 전자원부로 전환
제약사들이 의약품을 허가를 받을 때 종이로 발급됐던 각종 허가증 등이 온라인상 전자로 전환된다.
식약처는 2일 전자 허가증 관련 설명회를 갖고 관련 제도 도입에 따른 업무절차 등에 대해 제약사 등 관련 업체에 공유했다.
앞서 지난달 식약처는 '의약품 등의 안전에 관한 규칙 일부개정령안 입법예고하고 내년 1월 20일까지 의견조회를 진행중이다.
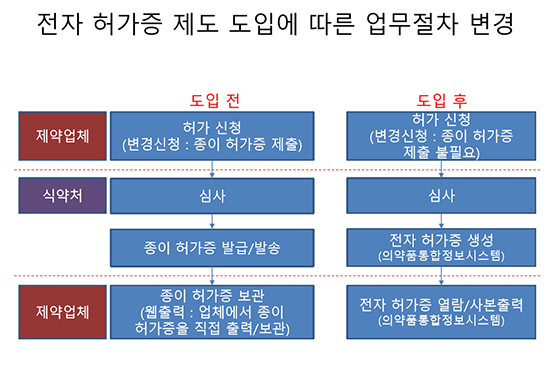
전자 허가증제도는 기존에 허가신청 또는 변경신청 시 종이 허가증을 제출했던 것을 온라인 '의약품통합정보시스템'을 통해 모든 절차를 진행하고 전자원부에서 관리하게 된다. 종이 허가증 제출이 불필요하게 된다.
내년에 본격적으로 시행될 제도는 완제의약품 제조수입업 품목허가 및 신고를 시작으로, 2021년 원료의약품 제조수입업 품목 허가·신고·등록, 2022년에는 GMP 적합판정 의약외품, 임상 관련 승인서 및 지정서로 확대될 예정이다.
식약처는 종이허가증 관련 수발신 비용이나 보관, 관리 등 각종 비용과 제출 소요 시간적 경제적 불편함을 해소하고 스마트폰 등으로 인한 정보 친화적 환경으로 의약품 등 허가증 웹 출력 방식을 선호해 해당 제도를 추진하게 됐다. 실제 지난해 기준 신규품목 85%가 웹 출력 방식을 선택했다는 게 식약처의 설명이다.

한편 전자원부는 허가, 신고, 등록 등과 그 변경에 관한 사항을 의약품통합정보시스템에 전자적 방법으로 기록, 등재, 관리, 보존하는 대장이다.
저작권자 © 뉴스더보이스헬스케어 무단전재 및 재배포 금지



